Антагонисты кальция тормозят вход ионов кальция внутрь клеток по потенциалзависимых кальциевых каналах.
Агонисты и антагонисты [ править | править код]
Агонист (рис. А) имеет сродство к рецептору, видоизменяет рецепторный белок, что в свою очередь влияет на функции клетки («внутренняя активность»). Биологическая эффективность агонистов, т. е. их влияние на функции клетки, зависит от того, насколько активация рецепторов может повлиять на передачу сигнала в клетке.
Рассмотрим два агониста А и В (рис. Б). Агонист А может вызвать максимальный эффект даже при связывании части рецепторов. Агонист В с таким же сродством, но с ограниченной способностью активировать рецептор (ограниченная внутренняя активность) и влиять на передачу сигнала может связываться со всеми рецепторами, но вызывает лишь ограниченный эффект, т. е. проявляет ограниченную эффективность. Агонист В является частичным агонистом. Потенциал агониста характеризуется концентрацией ЕС50, при которой достигается половина максимального эффекта.
Антагонисты (А) ослабляют действие агонистов: они влияют «антагонистически». Полные антагонисты имеют сродство к рецепторам, однако их связь не приводит к изменению клеточной функции (отсутствие внутренней активности). При одновременном применении агониста и полного антагониста результат их конкурентного действия определяется сродством и концентрацией каждого из этих веществ. Так, при повышении концентрации агониста, несмотря на противодействие антагониста, может быть достигнут полный эффект (рис. В): т. е. в присутствии антагониста кривая концентрация агониста — эффект смещается вправо по абсциссе к более высоким значениям концентрации. Модель молекулярного механизма действия агонистов/антагонистов (А)
Агонист вызывает переход в активную конформацию. Агонист присоединяется к неактивному рецептору и способствует его переходу в активную конформацию. Антагонист присоединяется к неактивному рецептору, при этом не меняя его конформацию.
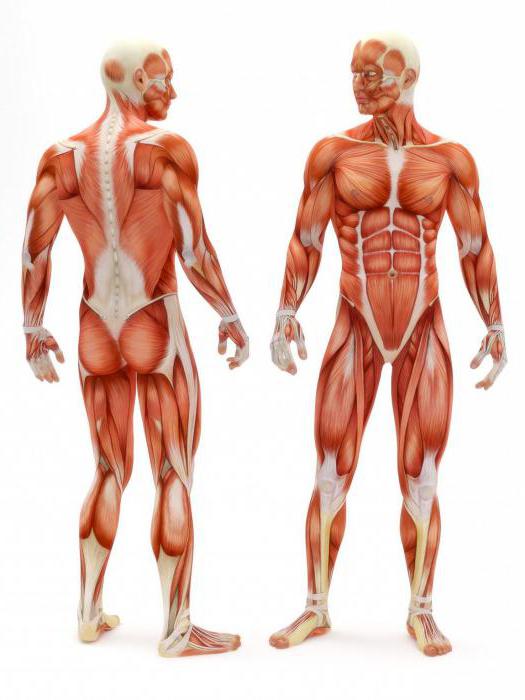
- Координация работы мышц
- РАБОТА МЫШЦ. ЭЛЕМЕНТЫ БИОМЕХАНИКИ …
- Мышцы-антагонисты, синергисты и …
- Мышцы-синергисты: примеры и описание
- Мышцы антагонисты и синергисты …
Агонист стабилизирует спонтанно возникающую активную конформацию. Рецептор может спонтанно перейти в активную форму. Однако статистическая вероятность такого события очень мала. Агонист селективно присоединяется к рецепторам, находящимся в активной конформации, и поддерживает это состояние рецептора. Антагонист обладает сродством к «неактивным» рецепторам и поддерживает их конформацию. Если спонтанная активность рецептора практически отсутствует, то введение антагониста не приводит к значимому эффекту. Если система имеет высокую спонтанную активность, антагонист оказывает действие, противоположное действию агониста: обратный агонист. «Истинный» антагонист без внутренней активности имеет одинаковое сродство как к активному, так и к неактивному рецептору и не влияет на исходную активность клетки. Частичный агонист не только селективно присоединяется к активному рецептору, но может частично связываться с неактивной формой. Другие формы антагонистического действия
Аллостерический антагонизм. Антагонист присоединяется к рецептору вне зоны присоединения агониста и снижает сродство агониста к этому рецептору. При аллостерическом синергизме сродство агониста усиливается.
Функциональный антагонизм. Два агониста посредством разных рецепторов влияют на один и тот же параметр (например, просвет бронхов) в противоположных направлениях (адреналин вызывает расширение, гистамин — сужение).
Разделение труда в нейрофизиологии сна: синхронизирующие и десинхронизирующие нервные центры
Нейроны каждого нервного центра контроля состояний сон/бодрствование имеют свой особенный характер импульсации. Одни нейроны, к примеру, активны только во время медленноволнового сна, другие — во время бодрствования. Возможны следующие варианты паттернов активности (рис. 3):
Рисунок 3. Варианты паттернов активности нервных центров, регулирующих цикл сон-бодрствование.
- Wake-on/REM-off — паттерн нейронов десинхронизирующих центров, индуцирующих и поддерживающих состояние бодрствования;
- REM-on — характерен для центров-десинхронизаторов, запускающих и поддерживающих фазу быстроволнового сна;
- NREM-on — свойственен нейронам синхронизирующих центров, под влиянием импульсации которых возникает медленноволновой сон;
- Wake-on/REM-on — паттерн нейронов, активных как во время быстроволнового сна, так и во время бодрствования.
Каждый центр представляет собой скопление нейронов, имеющих многочисленные связи с другими отделами головного мозга и использующих определенный нейромедиатор для передачи возбуждения (подробности на рис. 4) [4].
Рисунок 4. Локализация и паттерны импульсации нейронов нервных центров регуляции цикла сон-бодрствование. Рисунок составлен на основе [4].
Совокупность центров, обеспечивающих состояние бодрствования, называют восходящей возбуждающей системой (англ. ascendingarousalsystem, AAS). AAS состоит из моноаминергических, ацетилхолинергических нейронов и центров в латеральном гипоталамусе, секретирующих орексин (рис. 5) [5].
Рисунок 5. Расположение центров AAS. LC — locus coeruleus (голубое пятно), LDT — laterodorsal tegmental nucleus (заднелатеральное ядро покрышки), PPT — pedunculopontine nucleus (педункулопонтийное ядро покрышки), vPAG — ventral periaqueductal gray (передняя область центрального серого вещества), LH — lateral hypothalamus (латеральный гипоталамус), TMN — tuberomamillary nucleus (туберомамиллярное ядро гипоталамуса), BF — basal forebrain (базальный передний мозг). Рисунок из [5].
Рисунок 6. Реципрокные связи и самоингибирование моноаминергических нейронов в модели перехода от бодрствования и медленноволнового сна к быстроволновому сну. Стрелки на концах связующих линий обозначают возбуждение, «кирпичики» — торможение. Рисунок из [6].
Согласно принятой модели, смена состояний сон/бодрствование и фаз сна обусловлена двумя свойствами ответственных за это нервных центров (рис. 6):
- реципрокным торможением конкурирующих центров (например, моноаминергические тормозят ГАМК-ергические во время бодрствования);
- способностью к самоингибированию (активность нервного центра сама себя ограничивает и постепенно угасает, давая центру-конкуренту проявить себя) [6].
Упрощенная схема перехода от состояния бодрствования ко сну выглядит так: во время бодрствования моноаминергическая система тормозит ГАМК-ергические нейроны вентролатеральной преоптической области (ВЛПО), а нейроны ВЛПО, становясь активными во время сна, в свою очередь ингибируют моноаминергические нейроны.
Моноаминергические центры активируются возбуждающими импульсами из латерального гипоталамуса от нейронов, использующих орексин. Последние получают возбуждающие сигналы от нейронов лимбической системы, супрахиазмального ядра (СХЯ), гипоталамических структур, анализирующих и регулирующих энергетический баланс. Отсюда следует, что бодрствование зависит от эмоционального состояния (лимбическая система), циркадных ритмов (СХЯ) и энергетической обеспеченности организма.
Активированные моноаминергические нейроны посылают тормозящие обратные импульсы к орексиновым центрам. Такая обратная связь служит для поддержания бодрствования: как только падает активность орексиновых нейронов, снижается и активность моноаминергических. Тогда орексиновые нейроны возобновляют прежний поток возбуждающих залпов к моноаминергическим партнерам [7].
Таким образом сохраняется баланс, предотвращающий чрезмерное возбуждение моноаминергических нейронов и отдающий первенство в индуцировании бодрствования циркадным ритмам, эмоциям, энергетическому балансу организма и другим факторам (рис. 7).
Орексиновые нейроны в данной модели служат для стабилизации цикла сон-бодрствование: они не дают одному состоянию резко перейти в другое. Если убрать из модели орексиновые нейроны и оставить лишь ингибирующие друг друга ГАМК-ергические и моноаминергические, то переход от одного состояния к другому будет непредсказуемым и всецело зависящим от преобладающей активности той или иной системы. В экспериментах мыши с недостаточностью орексина не страдали избытком сна, однако могли внезапно перейти из состояния бодрствования в состояние сна. Подобные внезапные переходы ко сну характерны и для людей, страдающих нарколепсией [5, 7].
Рисунок 7. Схематическое изображение связей между латеральным гипоталамусом (орексин), моноаминергическими нейронами и ВЛПО (ГАМК). а — Бодрствование. Орексиновые нейроны получают возбуждающие импульсы из лимбической системы, супрахиазмального ядра и других областей гипоталамуса. Аксоны этих нейронов образуют с моноаминергическими клетками возбуждающие синапсы. Моноаминергические нейроны ингибируют активность нейронов ВЛПО и орексиновых нейронов. Снижение активности орексиновых нейронов ведет к снижению активности моноаминергических нейронов; тормозящее влияние последних ослабляется, и орексиновые клетки возобновляют прежний ритм импульсации к моноаминергическим нейронам. б — Сон. Нейроны ВЛПО активны и ингибируют как орексиновые, так и моноаминергические нейроны. в — Нарколепсия. Орексиновые нейроны отсутствуют, и состояние сна или бодрствования определяется преобладающей активностью моноаминергических или ГАМК-ергических нейронов. Переход между состояниями внезапен. Рисунок из [5].
Побочные действия антагонистов кальция
Вазодилатация дигидропиридинами вызывает рефлекторную активацию симпатической нервной системы, что ведет к возникновению тахикардии, ощущение прилива крови к лицу, вызывает гиперемию кожи лица, приступы стенокардии у больных ИБС, наджелудочковые аритмии, тибиального отеки, головная боль, головокружение, гипотонию.
Отрицательный ино, хроно и дромотропный эффекты фенилалкиламинов проявляются усилением симптомов сердечной недостаточности, брадикардией, нарушением проводимости.
- Мышцы антагонисты и синергисты …
- РАБОТА МЫШЦ. ЭЛЕМЕНТЫ БИОМЕХАНИКИ …
- Мышцы синергисты программа тренировок
- Что такое мышцы антагонисты, и как их …
- Что такое мышцы антагонисты, и как их …
Антагонисты кальция вызывают со стороны желудочно-кишечного тракта запоры, понос, тошноту, со стороны центральной нервной системы — депрессию, сонливость, бессонница, парестезии. Могут возникать при их применении и аллергические реакции.
Подтип 5-НТ1F
Из-за высокой гомологии (более 57%) с предыдущим подтипом его изучение также было затруднено по причине почти полного отсутствия селективных лигандов. Однако, в сноске из описания предыдущего подтипа есть ссылка на статью с описанием синтеза и методики скрининга новых соединений, обладающих высокой селективностью и к 5-HT1F-рецептору, одним из которых оказался 5-N-бутирилокси-ДМТ. В настоящее время высокая плотность 5-НТ1F-рецепторов обнаружена в таких областях мозга, как скорлупа, гиппокамп и хвостатое ядро.